PRACTICA LABORATORIO
Objetivos
- Obtener el acetileno a partir de carburo de calcio y agua
- Interpretar las reacciones de adicion y acidez de los productos
- Comparar el método de obtención del acetileno en el laboratorio e industrialmente
- Identificar cualitativamente por medio de reacciones especificas al acetileno.
- Acetileno y sus reacciones químicas.- Los alquinos son hidrocarburos alifáticos con al menos un triple enlace -C≡C- entre dos átomos de carbono. Se trata de compuestos metaestables debido a la alta energía del triple enlace carbono-carbono. Su fórmula general es CnH2n-2. El acetileno o etino es el alquino más sencillo. Es un gas, altamente inflamable, un poco más ligero que el aire e incoloro. Produce una llama de hasta 3.000 ºC, una de las temperaturas de combustión más altas conocidas, superada solamente por la del hidrógeno atómico (3400 ºC – 4000 ºC), el cianógeno (4525 ºC) y la del dicianoacetileno (4987 ºC).
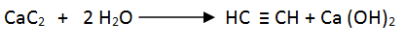
A nivel industrial, el acetileno se obtiene de la reacción del carburo de calcio con el agua, este proceso puede resumirse en dos pasos:
1.- El carburo de calcio (acetiluro de calcio), es un material grisáceo con aspecto de roca, se obtiene calentando óxido de calcio y coque (carbón) en un horno eléctrico a unos 3000°C.
2.- El carburo de calcio reacciona con el agua a temperatura ambiente produciendo acetileno.
Otro método es por la pirolisis del metano: El CH4 a altas temperaturas, se piroliza dando acetileno e hidrógeno.
El principal uso que se le da al acetileno es como combustible en el soplete oxiacetilénico, para soldar y cortar metales.




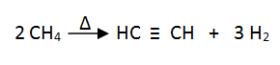





0 comentarios:
Publicar un comentario